DIAGNOSI E TERAPIE IN CASO DI ANOMALIE DEGLI SPERMATOZOI
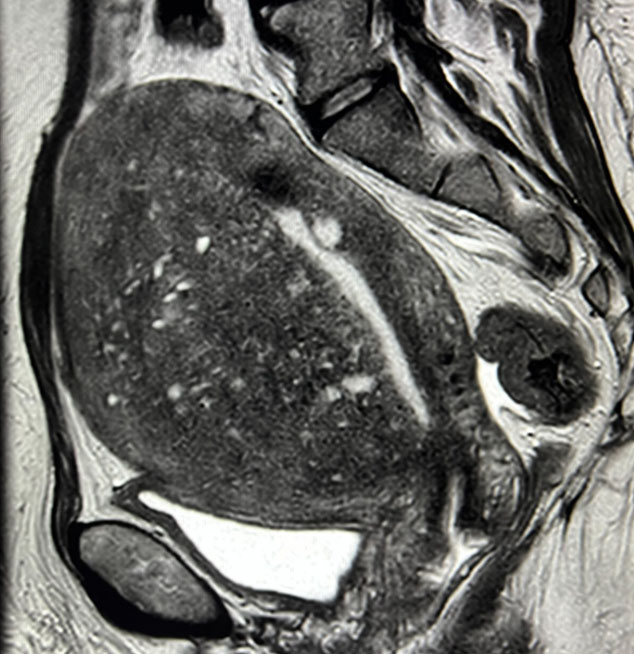
Reading Time: 5 minutesL’infertilità è un problema importante per la salute riproduttiva umana e colpisce circa il 15% delle coppie in tutto il mondo. L’infertilità può derivare da disturbi dello sviluppo sessuale o da disturbi endocrini della riproduzione con esordio nell’infanzia, nella prima infanzia o nell’adolescenza. L’infertilità maschile, che rappresenta circa la metà di tutti i casi di infertilità, si manifesta generalmente con una diminuzione del numero degli spermatozoi definita azoospermia o oligozoospermia, con un’attenuata motilità degli spermatozoi detta astenozoospermia o una percentuale maggiore di spermatozoi morfologicamente anomali, teratozoospermia. Queste caratteristiche degli spermatozoi, definite in termine di quantità/concentrazione nell’eiaculato, volume, morfologia e motilità vengono studiate nell’analisi dello sperma, chiamato spermiogramma. L’analisi pratica dello sperma segue le raccomandazioni del manuale di laboratorio dell’OMS per l’esame e il trattamento dello sperma umano. Lo scopo dell’analisi dello sperma è caratterizzare il potenziale di fertilità del maschio, che viene integrato da indagini cliniche ed endocrine prima che venga presa una decisione definitiva sulle opzioni di trattamento. In termini pratici, l’esecuzione dettagliata di un’analisi macroscopica e microscopica del liquido seminale è decisiva per ottenere risultati validi e successive decisioni terapeutiche. La qualità dello sperma è soggetta a influenze endocrine ed esterne che devono essere riconosciute e, se necessario, trattate. L’assunzione regolare di farmaci può influenzare l’asse del controllo ormonale (asse ipotalamo-ipofisi-gonadi). Le infezioni febbrili acute possono compromettere temporaneamente la spermatogenesi e provocare una ridotta qualità dello sperma, che di solito ritorna alla normalità dopo 3-6 mesi. Inoltre, il periodo di astinenza sessuale influisce sulla qualità dello sperma. Si consiglia pertanto di attendere “un’attesa” da 2 a 5 giorni prima della diagnosi dell’eiaculato e di documentare eventuali deviazioni da questa. Una breve astinenza sessuale inferiore a 48 ore può portare a una riduzione del numero degli spermatozoi; un’astinenza sessuale prolungata superiore a 7 giorni può, ad esempio, ridurre la motilità degli spermatozoi. L’eiaculato è costituito da 2 componenti principali: la porzione più piccola (ca. 5%) proviene dal testicolo ed è costituita principalmente da sperma, la porzione più grande (ca. 95%) è il plasma seminale, una miscela di liquidi dell’epididimo e del liquido seminale delle ghiandole sessuali accessorie (prostata e vescicole seminali). Il numero, la motilità e la morfologia degli spermatozoi sono i tre pilastri della valutazione dell’eiaculato, lo spermiogramma standard secondo l’OMS rileva anche il volume dell’eiaculato e il valore del pH, la vitalità degli spermatozoi, le cellule rotonde, i leucociti e gli autoanticorpi spermatici.
L’oligo-asteno-teratozoospermia (OAT) è frequentemente segnalata negli uomini provenienti da coppie infertili. L’eziologia alla base della TAO è nella maggior parte dei casi sconosciuta e una varietà di fattori che contribuiscono possono dare origine alla sindrome. Secondo la definizione data dall’OMS nel ‘Manuale di laboratorio dell’OMS per l’esame e il trattamento del seme umano’ (quinta edizione, 2010), per TAO si intende un campione di sperma con: presenza di spermatozoi nell’eiaculato ma il numero totale al di sotto del numero inferiore limite di riferimento, percentuale di spermatozoi progressivamente mobili (PR) al di sotto del limite di riferimento inferiore e percentuale di spermatozoi morfologicamente normali al di sotto del limite di riferimento inferiore.
Per quanto riguarda i trattamenti proposti, questi si basano su terapie farmacologiche mediche/integrative o chirurgiche. Tra queste ritroviamo la proposta del trattamento con FSH, il quale può essere suggerito con scarsa evidenza in uomini selezionati provenienti da coppie infertili, uomini normogonadotropi con oligozoospermia idiopatica o TAO, nel tentativo di migliorare i parametri quantitativi e qualitativi dello sperma e il tasso di gravidanza. Mentre l’FSH ricombinante (recFSH) o purificato umano (hpFSH) può essere utilizzato con successo per il trattamento dell’ipogonadismo ipogonadotropo, la sua applicazione all’infertilità maschile idiopatica è più controversa. Gli antiestrogeni, come tamoxifene e clomifene, sono ampiamente utilizzati da decenni per il trattamento dell’infertilità maschile idiopatica, portando ad un aumento significativo della concentrazione e della motilità degli spermatozoi, in assenza di effetti avversi significativi. In circa la metà degli uomini infertili si riscontra uno squilibrio tra stress ossidativo e capacità antiossidante nel plasma seminale. Le specie reattive dell’ossigeno (ROS) causano danni alle membrane degli spermatozoi mediante perossidazione lipidica che influisce sulla motilità degli spermatozoi e sulla reazione acrosomiale. Inoltre, portano ad una maggiore frammentazione del DNA. In una recente Cochrane Data Base Systemic Review del 2011 che comprendeva studi randomizzati e controllati su coppie che utilizzavano vari composti antiossidanti, è stato dimostrato un impatto positivo sui nati vivi e sul tasso di gravidanza nelle coppie subfertili sottoposte a cicli ART, ma un recente aggiornamento di questa revisione del 2014 ha concluso “che esistono prove di bassa qualità provenienti solo da piccoli studi randomizzati e controllati che suggeriscono che la supplementazione di antiossidanti nei maschi subfertili può migliorare i tassi di natalità vivi per le coppie che frequentano le cliniche della fertilità”. Prove di bassa qualità suggeriscono che i tassi di gravidanza clinica possono aumentare. Gli inibitori dell’aromatasi sono stati raccomandati agli uomini con parametri spermatici alterati e un basso rapporto testosterone/estrogeni. Diversi piccoli studi che hanno utilizzato letrozolo o anastrozolo hanno rivelato un aumento significativo dei parametri spermatici. Sebbene questi risultati siano molto promettenti, questo tipo di trattamento attualmente non può essere raccomandato in generale a causa del numero limitato di studi e delle dimensioni delle popolazioni studiate. Infine, i regimi terapeutici con androgeni non possono essere raccomandati, poiché diverse meta-analisi non sono riuscite a dimostrare alcun miglioramento nei tassi di gravidanza o nei parametri dello sperma negli uomini con infertilità idiopatica.
Nella oligo-asteno-teratozoospermia, la chirurgia può aiutare a rimuovere una causa di compromissione spermatogena (come il varicocele), a correggere i disturbi dello svuotamento del tratto seminale distale (dovuti a cisti intraprostatica o stenosi del dotto eiaculatorio), a migliorare i risultati dell’ICSI. Il trattamento del varicocele nelle coppie infertili che riferiscono TAO associata a varicocele palpabile può essere discusso con la coppia, prendendo in considerazione il monitoraggio solo nei casi con varicocele subclinico, trattando invece i giovani maschi con progressiva insufficienza testicolare e/o deterioramento seminale. La correlazione tra varicocele (uni- o bilaterale) e TAO è controversa, a causa della sua presenza sia negli uomini adulti con analisi dello sperma normale che negli uomini con TAO. Recenti meta-analisi mostrano un miglioramento della qualità dello sperma in seguito alla riparazione palpabile del varicocele, possibilmente con un tasso di concepimento più elevato dopo l’intervento chirurgico rispetto al mancato intervento chirurgico e diminuzione del danno al DNA spermatico. Inoltre, la varicocelectomia può aumentare il livello di testosterone totale negli uomini ipogonadici con subfertilità. Al contrario, nessun miglioramento significativo della fertilità postoperatoria è stato dimostrato nei casi di TAO associati a varicocele subclinico.
Finora, non ci sono prove sufficienti da studi interventistici reali che i cambiamenti nello stile di vita migliorino la fertilità maschile. Tuttavia, gli andrologi dovrebbero consigliare ai pazienti affetti da TAO di migliorare il loro stile di vita, con ulteriori benefici per la salute; eliminare il fumo per aumentare le possibilità della coppia di ottenere la gravidanza desiderata, ridurre il peso, ridurre il consumo di alcol, ridurre l’attività fisica se estrema.
È evidente che le possibilità di trattare efficacemente la TAO sono ancora piuttosto limitate, pertanto nel caso in cui altre opzioni di trattamento non siano disponibili o non siano efficaci, si raccomanda agli uomini con TAO e al loro partner di affidarsi alle tecniche di riproduzione assistita per aumentare le loro possibilità di ottenere una gravidanza.
Riferimenti
G M Colpi, et al. European Academy of Andrology guideline Management of oligo-astheno-teratozoospermia. Andrology. 2018 Jul;6(4):513-524. doi: 10.1111/andr.12502.
Sabine Kliesch. [“Practical spermiogram”-semen analysis according to WHO recommendations]. Urologe A. 2021 May;60(5):647-656. doi: 10.1007/s00120-021-01537-1. Epub 2021 Apr 30.
Shi-Ya Jiao et al. Molecular genetics of infertility: loss-of-function mutations in humans and corresponding knockout/mutated mice. Hum Reprod Update. 2021 Jan 4;27(1):154-189. doi: 10.1093/humupd/dmaa034.